hh khí A gồm H2 , N2 , CH4 . Trộn 150 ml khí A với 230 ml khí oxi . Sau khí đốt cháy và làm lạnh thấy còn 176 ml khí B còn lại lội qua dd NaOH dư thì còn lại 92 ml khí . Tính % về V mỗi khí trong A . Biết các khí trên đều đo ở cùng điều kiện

Những câu hỏi liên quan
Hh khí X gồm đimetylamin và hai hiđrocacbon đồng đẳng liên tiếp. Đốt cháy hoàn toàn 100 ml hh X bằng một lượng oxi vừa đủ, thu được 550 ml hh Y gồm khí và hơi nước. Nếu cho Y đi qua dd axit sunfuric đặc (dư) thì còn lại 250 ml khí (các thể tích khí và hơi đo ở cùng điều kiện). Công thức phân từ của hai hiđrocacbon là A. CH4 và C2H6. B. C2H4 và C3H6. C. C2H6 và C3H8. D. C3H6 và C4H8.
Đọc tiếp
Hh khí X gồm đimetylamin và hai hiđrocacbon đồng đẳng liên tiếp. Đốt cháy hoàn toàn 100 ml hh X bằng một lượng oxi vừa đủ, thu được 550 ml hh Y gồm khí và hơi nước. Nếu cho Y đi qua dd axit sunfuric đặc (dư) thì còn lại 250 ml khí (các thể tích khí và hơi đo ở cùng điều kiện). Công thức phân từ của hai hiđrocacbon là
A. CH4 và C2H6.
B. C2H4 và C3H6.
C. C2H6 và C3H8.
D. C3H6 và C4H8.
Đáp án B
Khi các chất khí đo ở cùng điều kiện thì tỉ lệ mol cũng là tỉ lệ thể tích
TH1: Hai anken

TH2: Hai ankan
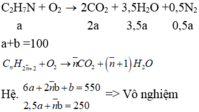
Đúng 0
Bình luận (0)
Đốt cháy 100 ml khí A cần vừa đủ 1375 ml không khí thu được 1700 ml khí, dẫn hh khí qua bình đựng CaCl2 khan thể tích khí còn lại 1350 ml, tiếp tục dẫn qua nước vôi trong dư thu được 1150 ml khí không bị hấp thụ. Tìm CTPT của A (biết các khí đo trong cùng đk) ĐS: C2H7NO2
Xin các cao nhân giúp đỡ
Cho 50ml lít Hiđrocacbon ở thể khí với 30ml lít oxi Lấy Du vào bình chứa lưu huỳnh khi đốt cháy hoàn toàn sản phẩm tạo thành được làm lạnh thì trong bình còn 200 ml khí trong đó có 150 ml khí bị hấp thụ bởi KOH phần khí còn lại bị hấp thụ bởi P hãy tìm cthh
Hình như để sai thiệt đó bạn. Minh tinh mai no no cu ra am. neu ra duong thi lai ra n=0
Đúng 0
Bình luận (0)
A là hh khí gồm CH4 , C2H4 và H2. Cho 3360 ml A sục qua dd brom thấy dd bị nhạt màu và khối lượng tăng thêm 0,84 g.a. Xác định % thể tích mỗi khí trong A. Biết rằng 0,7 lit hh khí này có khối lượng 0,4875g.b. Đốt cháy hoàn toàn 1,68 lít A rồi dẫn sản phẩm vào 1 lít dd Ca(OH) 2 0,05M ( D 1,025). Tính nồng độ % của chất sau phản ứng. Các thể tích khí đo ở đktc.
Đọc tiếp
A là hh khí gồm CH4 , C2H4 và H2. Cho 3360 ml A sục qua dd brom thấy dd bị nhạt màu và khối lượng tăng thêm 0,84 g.
a. Xác định % thể tích mỗi khí trong A. Biết rằng 0,7 lit hh khí này có khối lượng 0,4875g.
b. Đốt cháy hoàn toàn 1,68 lít A rồi dẫn sản phẩm vào 1 lít dd Ca(OH) 2 0,05M ( D= 1,025). Tính nồng độ % của chất sau phản ứng. Các thể tích khí đo ở đktc.
a) \(m_{tăng}=m_{C_2H_4}=0,84\left(g\right)\)
=> \(n_{C_2H_4}=\dfrac{0,84}{28}=0,03\left(mol\right)\)
Gọi số mol CH4, H2 trong 3360 ml A là a, b
=> \(a+b=\dfrac{3,36}{22,4}-0,03=0,12\left(mol\right)\) (1)
Gọi số mol CH4, H2 trong 0,7 lít hh là ak, bk
=> ak + bk + 0,03k = \(\dfrac{0,7}{22,4}=0,03125\) (2)
Và 16ak + 2bk + 0,84k = 0,4875 (3)
(1)(2)(3) => \(\left\{{}\begin{matrix}a=0,09\left(mol\right)\\b=0,03\left(mol\right)\\k=\dfrac{5}{24}\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,03}{0,15}.100\%=20\%\\\%V_{CH_4}=\dfrac{0,09}{0,15}.100\%=60\%\\\%V_{H_2}=\dfrac{0,03}{0,15}.100\%=20\%\end{matrix}\right.\)
b)
\(n_{C_2H_4}=\dfrac{1,68}{22,4}.20\%=0,015\left(mol\right)\)
\(n_{CH_4}=\dfrac{1,68}{22,4}.60\%=0,045\left(mol\right)\)
\(n_{H_2}=\dfrac{1,68}{22,4}.20\%=0,015\left(mol\right)\)
Bảo toàn C: \(n_{CO_2}=0,075\left(mol\right)\)
Bảo toàn H: \(n_{H_2O}=0,135\left(mol\right)\)
\(n_{Ca\left(OH\right)_2}=0,05.1=0,05\left(mol\right)\)
\(m_{ddCa\left(OH\right)_2}=1000.1,025=1025\left(g\right)\)
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
0,05---->0,05----->0,05
CaCO3 + CO2 + H2O --> Ca(HCO3)2
0,025<--0,025------------>0,025
\(m_{CaCO_3}=\left(0,05-0,025\right).100=2,5\left(g\right)\)
mdd sau pư = 1025 + 0,075.44 + 0,135.18 - 2,5 = 1028,23 (g)
\(C\%_{Ca\left(HCO_3\right)_2}=\dfrac{0,025.162}{1028,23}.100\%=0,3939\%\)
Đúng 3
Bình luận (0)
Cho 400 ml một hỗn hợp gồm nitơ và một hiđrocacbon vào 900 ml oxi (dư) rồi đốt. Thể tích hỗn hợp thu được sau khi đốt là 1,4 lít. Sau khi cho nước ngưng tụ còn 800 ml hỗn hợp, người ta cho lội qua dung dịch KOH thấy còn 400 ml khí. Các thể tích khí đều đo ở cùng điều kiện nhiệt độ, áp suất. Công thức phân tử của chất hữu cơ là
Cho 400 ml một hỗn hợp gồm nito và một hidrocacbon vào 900 ml oxi (dư) rồi đốt. Thể tích hỗn hợp thu được sau khi đốt là 1,4 lít. Sau khi cho nước ngưng tụ còn 800 ml hỗn hợp, người ta cho lội qua dung dịch KOH thấy còn 400 ml khí. Các thể tích khí đều đo ở cùng điều kiện nhiệt độ, áp suất. Xác định CTPT chất hữu cơ
Ta có: \(V_{H_2O}=1400-800=600\left(ml\right)\)
\(V_{O_2\left(dư\right)}+V_{N_2}=400\left(ml\right)\)
\(\Rightarrow V_{CO_2}=800-400=400\left(ml\right)\)
BTNT O, có: \(V_{O_2\left(pư\right)}=\dfrac{2V_{CO_2}+V_{H_2O}}{2}=700\left(ml\right)\)
\(\Rightarrow V_{O_2\left(dư\right)}=900-700=200\left(ml\right)\) \(\Rightarrow V_{N_2}=400-200=200\left(ml\right)\)
\(\Rightarrow V_{C_xH_y}=400-200=200\left(ml\right)\)
\(\Rightarrow\left\{{}\begin{matrix}x=\dfrac{V_{CO_2}}{V_{C_xH_y}}=2\\y=\dfrac{2V_{H_2O}}{V_{C_xH_y}}=6\end{matrix}\right.\)
Vậy: CTPT của X là C2H6.
Đúng 1
Bình luận (0)
Cho 400 ml một hỗn hợp gồm nito và một hidrocacbon vào 900 ml oxi (dư) rồi đốt. Thể tích hỗn hợp thu được sau khi đốt là 1,4 lít. Sau khi cho nước ngưng tụ còn 800 ml hỗn hợp, người ta cho lội qua dung dịch KOH thấy còn 400 ml khí. Các thể tích khí đều đo ở cùng điều kiện nhiệt độ, áp suất. Xác định CTPT chất hữu cơ
Đốt cháy 50 ml hỗn hợp khí X gồm trimetylamin và 2 hiđrocacbon là đồng đẳng liên tiếp bằng oxi vừa đủ, thu được 375 ml hỗn hợp khí và hơi Y. Cho Y đi qua
H
2
S
O
4
đặc dư thì còn lại 175 ml, các thể tích khí đo ở cùng điều kiện. CTPT của 2 hiđrocacbon là A.
C
2
H
6
;
C...
Đọc tiếp
Đốt cháy 50 ml hỗn hợp khí X gồm trimetylamin và 2 hiđrocacbon là đồng đẳng liên tiếp bằng oxi vừa đủ, thu được 375 ml hỗn hợp khí và hơi Y. Cho Y đi qua H 2 S O 4 đặc dư thì còn lại 175 ml, các thể tích khí đo ở cùng điều kiện. CTPT của 2 hiđrocacbon là
A. C 2 H 6 ; C 3 H 8 .
B. C 2 H 4 ; C 3 H 6 .
C. C 3 H 6 v à C 4 H 8 .
D. C 3 H 8 v à C 4 H 10 .
Ta có: V H 2 O = 375 – 175 = 200 m l ; V C O 2 + V N 2 = 175 m l
V H 2 O − V H 2 O − V N 2 = 25 m l = 1 2 n h h
→ 2 hiđrocacbon chỉ có thể là anken và V a m i n = V a n k e n = 25 m l
Đặt công thức chung của 2 anken là C n ¯ H 2 n ¯ + 2
V C O 2 = 25 n ¯ + 3.25 = 25 n ¯ + 75 ; V N 2 = 0 , 5.25 = 12 , 5
→ 25 n ¯ + 75 + 12,5 = 175 → n ¯ = 3,5
Vậy 2 hiđrocacbon là C 3 H 6 v à C 4 H 8
Đáp án cần chọn là: C
Đúng 0
Bình luận (0)
,Thên từ từ Mg vào 100 ml dd A tới khi khí ngừng thoát ra thu dc dd B (V 100ml) chỉ chưa các muối của Mg và 0,963 l hồn hợp D gồm 3 khí ko màu cân nặng 0,772 g.Trộn khí D với 1 lít khí oxi sau khi pu hoàn toàn cho khí còn lại đi qua dd NaOH dư thì thể tích hỗn hợp khí còn lại là 1,291 lít.a/Hỏi hỗn hợp D có những khí gì ?biết rằng trong khí D có 2 khí chiếm % thể tích như nhau đo ởđktc?b/Tinh CM các chất trong B và khối lượng Mg đã bị tan
Đọc tiếp
,Thên từ từ Mg vào 100 ml dd A tới khi khí ngừng thoát ra thu dc dd B (V= 100ml) chỉ chưa các muối của Mg và 0,963 l hồn hợp D gồm 3 khí ko màu cân nặng 0,772 g.Trộn khí D với 1 lít khí oxi sau khi pu hoàn toàn cho khí còn lại đi qua dd NaOH dư thì thể tích hỗn hợp khí còn lại là 1,291 lít.
a/Hỏi hỗn hợp D có những khí gì ?biết rằng trong khí D có 2 khí chiếm % thể tích như nhau đo ởđktc?
b/Tinh CM các chất trong B và khối lượng Mg đã bị tan














